重組蛋白驗證抗體的實驗流程
日期:2026-04-10 16:05:33
驗證重組蛋白的抗體,核心目標是確認該抗體能夠特異性識別你的目標蛋白,且不與宿主細胞蛋白(如大腸桿菌或HEK293T內源性蛋白)發生交叉反應。
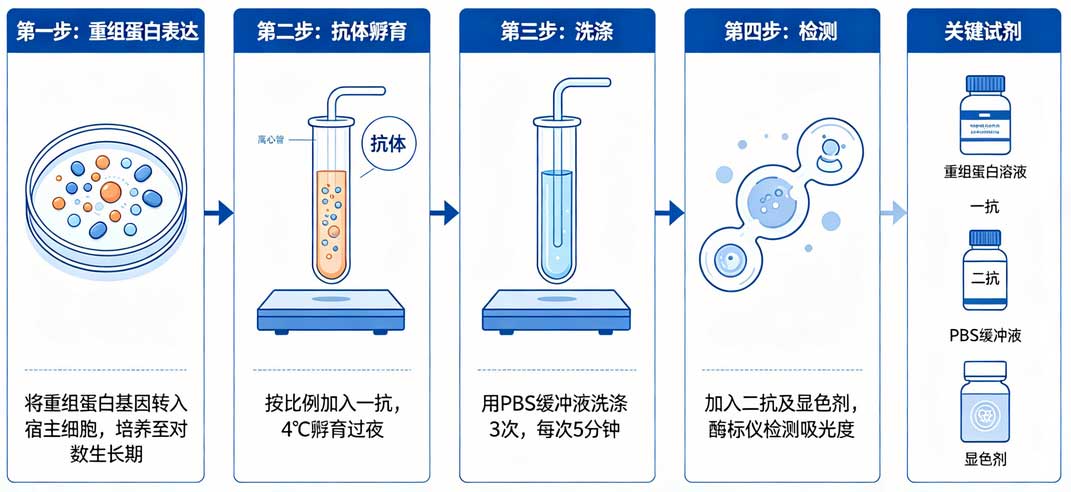

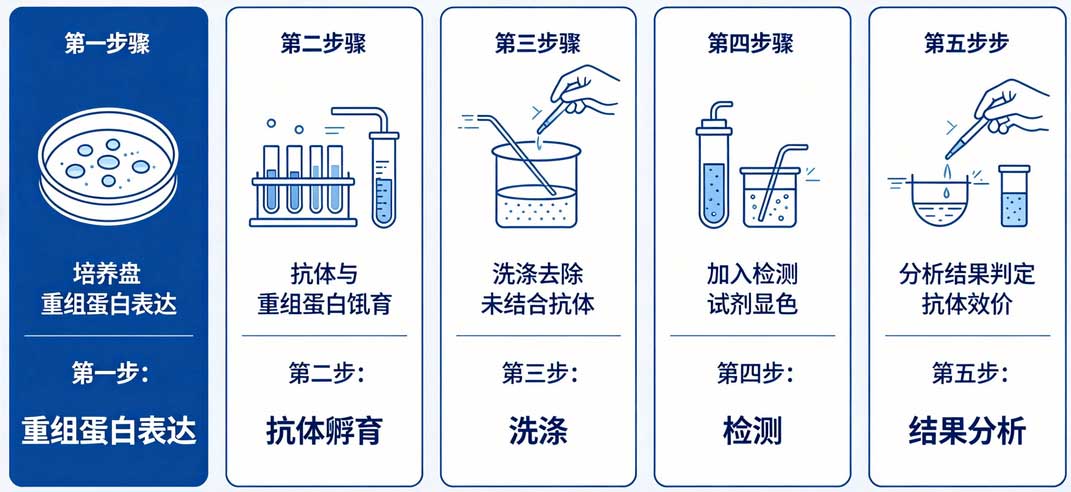
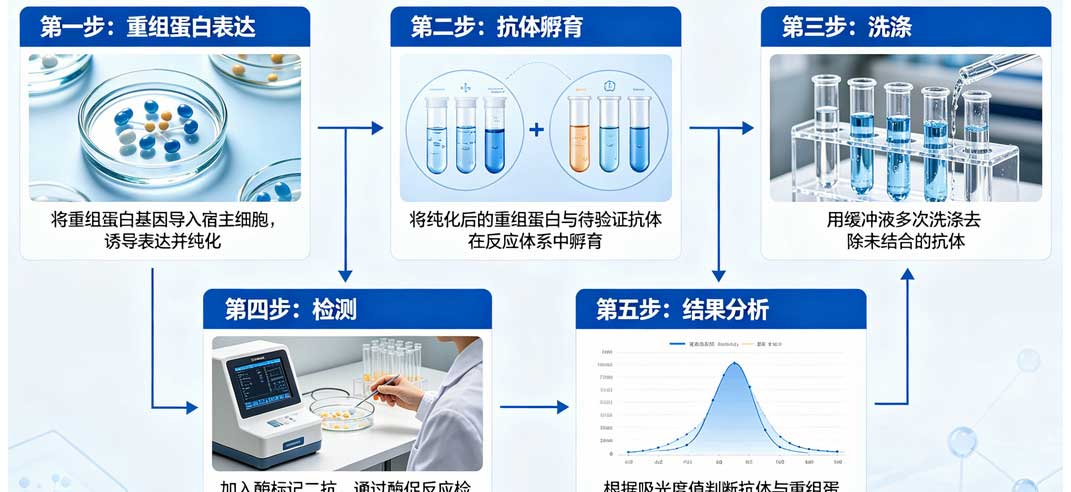
實驗流程,主要分為樣品制備、核心驗證實驗(Western Blot)、特異性確證以及定量評估四個階段。

第一階段:樣品制備與對照設置
實驗成功的關鍵在于對照組的設置。你需要準備以下三類樣品,以便在后續實驗中通過對比來排除干擾:
陽性樣品(目標蛋白):
純化蛋白: 表達并純化后的重組蛋白,溶解在適當的緩沖液中。
細胞裂解液: 轉染了帶有目標標簽(如His, Flag, GST)重組質粒的細胞裂解液。
陰性對照(背景參照):
空載體/未轉染細胞: 使用與陽性樣品相同的宿主細胞(如未轉染的HEK293T或大腸桿菌),經過相同的處理流程。這是為了證明抗體不會識別宿主細胞的內源性蛋白。
競爭抑制對照(可選,用于高嚴謹驗證):
準備過量的游離標簽肽段(如His肽段),用于后續的阻斷實驗。

第二階段:核心驗證實驗(Western Blot)
這是驗證重組蛋白抗體最常用、最直觀的方法,能夠同時評估抗體的特異性和分子量準確性。
1. 電泳與轉膜
將上述制備的陽性樣品和陰性對照樣品進行SDS-PAGE電泳。
注意: 如果你的重組蛋白以包涵體形式存在,需先進行變性處理;如果是分泌型蛋白,需檢測上清液。
將蛋白轉移至PVDF或NC膜上。
2. 抗體孵育(棋盤法滴定)
不要只使用說明書推薦的稀釋度。建議采用“棋盤滴定法”,設置一抗和二抗的梯度稀釋(例如一抗從1:500到1:5000,二抗從1:2000到1:10000)。
這能幫你找到信噪比(S/N)最高的最佳工作濃度。
3. 顯影與結果判定
使用ECL化學發光顯影。
合格標準:
在陽性樣品泳道中,在預期的分子量位置出現清晰、單一的條帶。
在陰性對照泳道中,該位置無條帶,且背景干凈。
如果陰性對照出現雜帶,說明抗體與宿主蛋白有交叉反應,需更換抗體或優化封閉條件。

第三階段:特異性確證(競爭抑制實驗)
為了進一步證明抗體識別的確實是你的目標標簽或蛋白,而非非特異性吸附,你需要進行競爭抑制實驗(Competitive Inhibition Assay)。
預孵育: 將抗體與過量的游離抗原肽段(Immunogen/Peptide)在室溫下孵育30-60分鐘。這會讓抗體的結合位點被“堵住”。
檢測: 用這管“被堵住”的抗體去孵育Western Blot膜(或進行ELISA/IF)。
判定: 如果原本的陽性條帶信號顯著減弱或完全消失,則證明抗體是特異性結合目標表位的。如果信號沒有變化,說明之前的條帶可能是非特異性結合。
第四階段:定量評估與效價測定(ELISA)
如果需要知道抗體的具體效價(即抗體能稀釋多少倍仍有效),ELISA是“金標準”。
包被: 使用高純度的重組蛋白抗原包被酶標板。
梯度稀釋: 將待測抗體進行大范圍的梯度稀釋(如從1:100稀釋至1:100,000)。
檢測: 加入酶標二抗并顯色,使用酶標儀讀取OD值。
效價判定: 以OD值大于空白對照2.1倍(或根據具體Cut-off值計算)時的最高稀釋倍數作為該抗體的效價。

關鍵注意事項
標簽的選擇: 驗證重組蛋白時,使用抗標簽抗體(如Anti-His, Anti-Flag)通常比抗蛋白特異性抗體更準確,因為標簽序列已知且無宿主背景干擾。
批次差異: 多克隆抗體不同批次間差異較大,每次更換新批次抗體時,建議重新進行上述驗證流程。
避免假陽性: 在Western Blot中,如果重組蛋白發生降解,可能會出現多條低分子量條帶;如果發生聚合,可能出現高分子量條帶。需結合蛋白特性進行區分。
上一篇: 跨膜蛋白表達純化技術解析
下一篇: 最后一頁














